4 Etude d'un réfrigérateur domestique
Les élèves ont déjà utilisé un réfrigérateur domestique, mais peu savent comment il marche... Le problème peut leur être posé dans ces termes :
on cherche à refroidir à - 5 °C (freezer) une enceinte située dans une pièce à la température ambiante de 20 °C environ ;
on leur demande de préciser tout d'abord comment on peut envisager d'opérer sachant que la chaleur ne s'écoule que dans le sens des températures décroissantes, puis de proposer un cycle qui permette de réaliser le transfert.
L'exercice peut être posé comme une situation-problème afin de susciter un débat scientifique dans la classe, ce qui permet de vérifier la manière dont les élèves raisonnent sur le plan de l'analyse physique des phénomènes. La figure ci-dessous permet de bien faire comprendre aux élèves que le deuxième principe de la thermodynamique est bien respecté : pour refroidir l'enceinte froide, on le met en contact avec un fluide qui est lui-même à température inférieure. Par une opération qui n'est pas encore précisée, ce fluide est porté à une température supérieure à celle du milieu environnant, dans lequel la chaleur est rejetée.
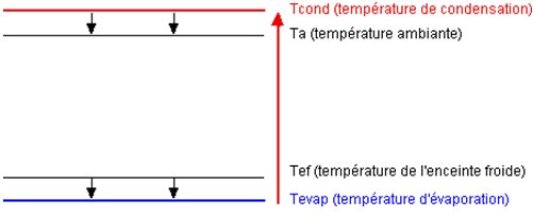
Cette figure illustre les transferts énergétiques qui prennent place dans le cycle. Les petites flèches dirigées vers le bas représentent les échanges thermiques, qui, comme on le voit, respectent bien le second principe de la thermodynamique : la chaleur s'écoule des températures chaudes vers les températures froides. La longue flèche ascendante représente l'apport enthalpique au compresseur, qui permet de relever le niveau de température du fluide (les énergies mises en jeu ne sont pas proportionnelles à la longueur des flèches).
Il est bien évidemment possible de modéliser directement ce cycle dans Thermoptim. Nous ne détaillerons pas ici complètement cette manière d'opérer, qui est bien documentée dans le guide de prise en mains relatif à un cycle frigorifique simple ou bien dans la séance Diapason S31 .
Nous en donnerons seulement un bref aperçu, après avoir présenté une manière de faire plus progressive qui peut bien convenir à des élèves débutants si l'enseignant souhaite qu'ils comprennent bien la manière dont les calculs sont effectués. Nous montrerons comment les élèves peuvent calculer le cycle pas à pas en procédant de deux manières différentes : tout d'abord en utilisant le calculateur-inverseur des propriétés des fluides, qui permet de ne pas faire appel à Thermoptim dans un premier temps, et ensuite en créant des points dans le progiciel. Une fois les points du cycle déterminés, ils peuvent être tracés dans les diagrammes thermodynamiques interactifs.
Cette manière de faire, qui diffère de la modélisation directe dans Thermoptim, présente sur le plan pédagogique l'intérêt que la démarche méthodologique de calcul d'un cycle doit être suivie de manière plus détaillée.
4.1 Présentation du cycle
le principe consiste à évaporer un fluide frigorigène à basse pression (et donc basse température), dans un échangeur en contact avec l'enceinte froide. Pour cela, il faut que la température Tevap (environ - 10 °C) du fluide frigorigène soit inférieure à celle Tef de l'enceinte froide (- 5 °C). Sur le plan technologique, l'échangeur de chaleur ayant une dimension finie, le fluide frigorigène ne peut en effet être à la même température que l'enceinte froide, mais on peut dans un premier temps considérer que l'échange de chaleur est bien isotherme ;
le fluide est ensuite comprimé à une pression telle que sa température de condensation Tcond (35 °C) soit supérieure à la température ambiante Ta (20 °C). Cette compression peut en première approximation être supposée adiabatique, pour les raisons évoquées dans l'introduction, mais non pas isentropique, compte tenu des irréversibilités qui prennent place dans le compresseur ;
il est alors possible de refroidir le fluide par échange thermique avec l'air ambiant, jusqu'à ce qu'il devienne liquide. Toutefois, le refroidissement ne peut généralement pas être isotherme, compte tenu des propriétés thermodynamiques des réfrigérants : il faut d'abord désurchauffer la vapeur, puis la condenser ;
le liquide est ensuite détendu à la basse pression, et dirigé dans l'évaporateur. Le cycle est ainsi refermé. En théorie, il serait possible de réaliser une détente proche de l'isentropique, mais la réalité technologique est autre, et ceci pour trois raisons : d'une part la détente d'un mélange diphasique se fait, sauf précautions particulières, avec un mauvais rendement isentropique, d'autre part le travail mis en jeu reste très faible, et enfin, surtout pour les machines frigorifiques de petite puissance, il n'existe pas de machine de détente appropriée et bon marché. C'est pourquoi en pratique on a recours à des détendeurs ou même à de simples capillaires, dispositifs statiques qui réalisent un laminage isenthalpique.
Le schéma de la machine (figure ci-dessous) se déduit de ces considérations.
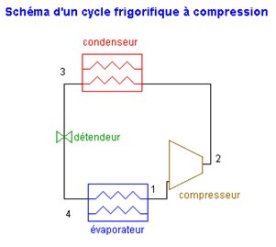
Dans l'exemple qui nous intéresse, les données du problème sont les suivantes : le fluide choisi est du R134a, hydrofluorocarbure de substitution aux CFC qui présente l'avantage d'avoir un potentiel de destruction de la couche d'ozone nul (c'est bien sûr l'occasion d'avoir une petite discussion sur ce sujet avec les élèves, et de faire le lien avec les préoccupations environnementales actuelles).
Compte tenu des températures d'évaporation et de condensation désirées, le cycle de réfrigération par compression de R134a fonctionne entre une pression d'évaporation de 2 bars et une pression de condenseur de 9 bars.
4.2 Technologie des composants
Une fois le schéma de principe de la machine défini (figure ci-dessus), la discussion peut porter sur les technologies des divers composants. Dans ce cas, cela revient à présenter les quatre éléments qui composent la machine. Si un réfrigérateur réel peut être montré aux élèves, c'est le mieux, sinon il est possible de leur demander, préalablement à l'exercice, d'avoir observé par eux-mêmes leur réfrigérateur familial.
Nous recommandons aussi de présenter aux élèves l'animation réalisée par Paraschool pour illustrer le fonctionnement d'un réfrigérateur domestique, intitulée : Voyage au cœur d'un réfrigérateur .
L'évaporateur est généralement, dans un réfrigérateur domestique, formé de deux plaques planes corruguées soudées l'une contre l'autre, le fluide frigorigène circulant dans les canaux formés par les corrugations. Il tapisse le plus souvent le compartiment « congélation » du réfrigérateur (c'est sur lui que se forme la couche de givre). La plaque entre les canaux de passage du fluide sert d'ailette pour augmenter le contact thermique entre le fluide frigorigène et le compartiment froid. Cet évaporateur est relié au reste de la machine par deux canalisations qui traversent la paroi isolante. L'une d'entre elles est reliée à l'aspiration du compresseur, l'autre au détendeur.
Le condenseur est la grille noire située sur la face postérieure du réfrigérateur, constituée d'un tuyau enroulé en serpentin et étayé par des plaques métalliques qui d'une part augmentent les échanges thermiques avec l'air, et d'autre part renforcent la rigidité mécanique. Sur le plan thermique, il est en fait composé de deux parties : la première, appelée désurchauffeur, sert à refroidir le fluide à l'état de vapeur, et la seconde, le condenseur proprement dit, à le condenser à l'état liquide.
Ces trois éléments transfèrent de la chaleur entre la machine et l'extérieur. Ce sont des dispositifs fixes, traversés par le fluide. Les pertes de charge y étant très faibles, leur comportement est en première approximation isobare. Les parois étant fixes, il n'y a pas de travail échangé avec l'extérieur, et l'application du premier principe en système ouvert[1] (
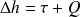 ) indique que la chaleur échangée est égale à la variation d'enthalpie du fluide entre l'entrée et la sortie :
) indique que la chaleur échangée est égale à la variation d'enthalpie du fluide entre l'entrée et la sortie :
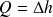 .
.
Le condenseur est relié à la sortie du compresseur et au détendeur.
Le plus souvent, le compresseur n'est pas directement visible car il est contenu dans un bloc métallique monté sur des coussins en caoutchouc, pour éviter les vibrations, d'où sortent un fil électrique et deux tuyaux d'entrée et sortie du fluide. Il s'agit d'un compresseur dit hermétique, à piston, qui présente l'avantage que le moteur est directement refroidi et lubrifié par le fluide thermodynamique, ce qui permet de se passer d'huile.
Pour éviter d'aspirer du liquide dans le compresseur, ce qui risquerait de le détruire car le liquide est incompressible, le gaz est surchauffé de 5 K au-dessus de la température de saturation avant d'entrer dans le compresseur. La surchauffe se fait pour partie par échange avec l'environnement.
Le compresseur est une machine compacte, traversée par le fluide à l'état gazeux. Les coefficients d'échange sont faibles, la surface d'échange réduite, de telle sorte que les échanges de chaleur sont en première approximation négligeables : le compresseur est adiabatique et l'application du premier principe indique que le travail de compression est égal à la variation d'enthalpie du fluide entre l'entrée et la sortie :
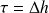 . Si la machine était parfaite, l'évolution du fluide serait isentropique, de travail de compression
. Si la machine était parfaite, l'évolution du fluide serait isentropique, de travail de compression
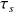 . En fait, il y a des irréversibilités, qui sont prises en compte par un rendement isentropique égal à 0,8. Cela signifie que le travail de compression réel est
. En fait, il y a des irréversibilités, qui sont prises en compte par un rendement isentropique égal à 0,8. Cela signifie que le travail de compression réel est
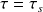 /0,8.
/0,8.
Le détendeur est généralement constitué d'un simple tube capillaire, et quelquefois il s'agit d'un détendeur thermostatique. Avant d'entrer dans le détendeur, le liquide est sous-refroidi de 5 K ; cela permet de s'assurer que cet organe n'est pas alimenté avec de la vapeur, et cela augmente les performances du réfrigérateur, comme on l'expliquera plus loin.
Le détendeur est un organe fixe, de petite taille, en première approximation adiabatique. Il n'y a donc ni chaleur ni travail échangé avec l'extérieur et l'application du premier principe indique que l'enthalpie du fluide est la même à l'entrée et à la sortie (
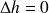 ). Il s'agit d'un laminage isenthalpique.
). Il s'agit d'un laminage isenthalpique.
4.3 Calcul du cycle pas à pas avec le calculateur-inverseur
Pour calculer ce cycle pas à pas, nous commencerons par utiliser le calculateur inverseur, sachant que le principal intérêt qu'il y a à procéder ainsi est d'une part de bien décomposer les différentes étapes et d'autre part de ne pas avoir dans un premier temps à introduire Thermoptim.
4.3.1 ETAT DU POINT 1
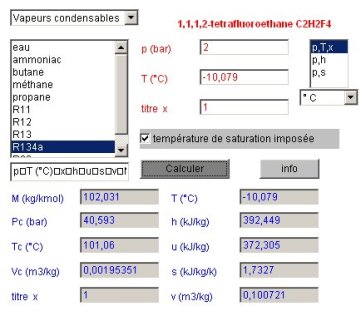
Pour déterminer l'état du point 1, il faut commencer par paramétrer le calculateur conformément à la figure du calculateur donnée ci-dessous. Le fluide sélectionné est le R134a, parmi les vapeurs condensables. Le calculateur doit être en mode de calcul (p,T,x) la pression étant égale à 2 bars, et la température de saturation imposée. Ce premier calcul permet de déterminer la température de saturation, égale ici à -10,079 °C. Le point 1 correspondant à une surchauffe de 5 K, sa température, qui vaut -5,079 °C, peut être entrée dans le calculateur ce qui permet, en décochant l'option "température de saturation imposée", de déterminer son état. Un copier-coller depuis le champ des résultats fournit les valeurs suivantes (p et Pc sont en bar, h et u en kJ/kg, s en kJ/kg/K, v et Vc en m3/kg, M en kg et Tc en K) :
P | T (°C) | x | h | u | s | v | M | Pc | Tc | Vc |
2 | -5,079 | 1 | 397,005 | 376,403 | 1,7499 | 0,103012 | 102,031 | 40,593 | 101,06 | 0,00195351 |
4.3.2 ETAT DU POINT 2s
Pour connaître l'état du point 2s, correspondant à la compression isentropique, le calculateur doit être paramétré en mode de calcul (p,s) la nouvelle pression étant égale à 9 bars, et l'entropie étant celle du point 1. Le calcul conduit à la figure ci-dessous.
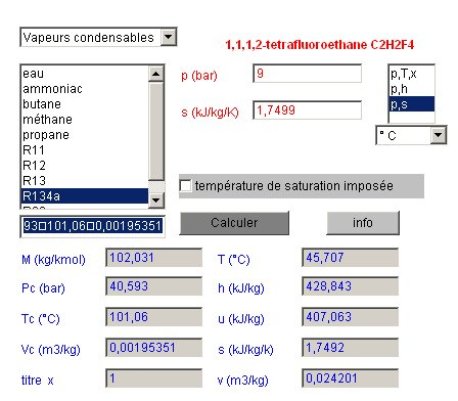
Un copier-coller depuis le champ des résultats fournit les valeurs suivantes, la valeur de l'entropie différant très légèrement du fait de la précision d'inversion des calculs.
P | T (°C) | x | h | u | s | v | M | Pc | Tc | Vc |
9 | 45,707 | 1 | 428,843 | 407,063 | 1,7492 | 0,024201 | 102,031 | 40,593 | 101,06 | 0,00195351 |
La variation d'enthalpie correspondant à la détente réversible est égale à h2s – h1, soit
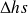 = 31,838 kJ/kg. Sa valeur positive provient des conventions utilisées en thermodynamique, le travail étant reçu de l'extérieur du système considéré.
= 31,838 kJ/kg. Sa valeur positive provient des conventions utilisées en thermodynamique, le travail étant reçu de l'extérieur du système considéré.
La valeur du travail de compression réel
 est, par définition du rendement isentropique
est, par définition du rendement isentropique
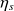 , égal à
, égal à
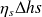 soit :
soit :
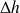 = 31,838/0,8 kJ/kg = 39,7975 kJ/kg
= 31,838/0,8 kJ/kg = 39,7975 kJ/kg
L'enthalpie du point 2 est donc égale à celle du point 1 plus
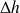 , soit 436,8025 kJ/kg
, soit 436,8025 kJ/kg
4.3.3 ETAT DU POINT 2
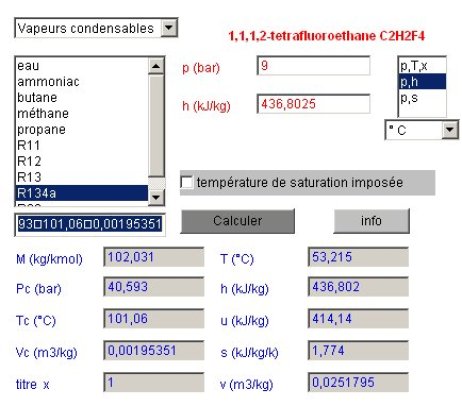
Pour connaître l'état du points 2, le calculateur doit être paramétré en mode de calcul (p,h) la pression restant égale à 9 bars, et l'enthalpie étant celle du point 436,8025. Le calcul conduit à la figure ci-dessous, et un copier-coller depuis le champ des résultats fournit les valeurs suivantes :
P | T (°C) | x | h | u | s | v | M | Pc | Tc | Vc |
9 | 53,215 | 1 | 436,802 | 414,14 | 1,774 | 0,0251795 | 102,031 | 40,593 | 101,06 | 0,00195351 |
4.3.4 ETATS DU POINT 3a
En sortie du compresseur, le fluide est condensé. Pour cela, il commence par être désurchauffé de la température T2 à la température de saturation à la pression de 9 bars (point 3a).
Pour connaître l'état du points 3a, le calculateur doit être en mode de calcul (p,T,x) la pression restant égale à 9 bars, et la température de saturation étant imposée, x valant 1. Un copier-coller depuis le champ des résultats fournit les valeurs suivantes :
P | T (°C) | x | h | u | s | v | M | Pc | Tc | Vc |
9 | 35,546 | 1 | 417,569 | 397,029 | 1,7131 | 0,0228222 | 102,031 | 40,593 | 101,06 | 0,00195351 |
4.3.5 ETAT DU POINT 3
Pour connaître l'état du point 3, le calculateur doit être en mode de calcul (p,T,x) la pression restant égale à 9 bars, et la température de saturation n'étant plus imposée, et T étant égale à T3a - 5K. Un copier-coller depuis le champ des résultats fournit les valeurs suivantes :
P | T (°C) | x | h | u | s | v | M | Pc | Tc | Vc |
9 | 30,546 | 0 | 242,598 | 241,838 | 1,1461 | 0,000844166 | 102,031 | 40,593 | 101,06 | 0,00195351 |
4.3.6 ETAT DU POINT 4
Pour connaître l'état du points 4, le calculateur doit être paramétré en mode de calcul (p,h) la nouvelle pression étant celle d'évaporation, égale à 2 bars, et l'enthalpie étant celle du point 3. Un copier-coller depuis le champ des résultats fournit les valeurs suivantes :
P | T (°C) | x | h | u | s | v | M | Pc | Tc | Vc |
2 | -10,079 | 0,27176 | 242,598 | 237,014 | 1,1631 | 0,02792 | 102,031 | 40,593 | 101,06 | 0,00195351 |
La valeur de la chaleur Q extraite à l'évaporateur vaut :
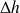 = h1 - h4 = 397 - 242,6 kJ/kg = 154,4 kJ/kg
= h1 - h4 = 397 - 242,6 kJ/kg = 154,4 kJ/kg
4.3.7 BILAN GLOBAL DU CYCLE
Les calculs précédents ont permis d'estimer la chaleur Q extraite à l'évaporateur (154,4 kJ/kg), et le travail de compression
 (39,8 kJ/kg).
(39,8 kJ/kg).
Le COefficient de Performance COP du cycle est égal au rapport de ces deux valeurs. Il vaut donc 154,4/39,8 = 3,89.
4.4 Calcul du cycle pas à pas avec les points de Thermoptim
Les écrans des points de Thermoptim permettent de faire les mêmes calculs que ceux que nous venons d'effectuer. Comme nous allons le voir, les résultats sont identiques, mais cela suppose de tout de suite initier les élèves à une partie des fonctionnalités du simulateur.
Tant que l'on ne définit pas les transfos, l'éditeur de schémas ne doit pas être utilisé. Les points peuvent en effet être directement créés depuis l'écran du simulateur, en double-cliquant sur le bandeau de la table des points. Une fois qu'un point existe, le bouton « Dupliquer » permet d'en générer un autre sans avoir à entrer le corps.
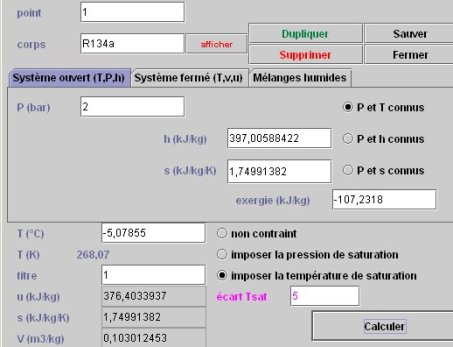
4.4.1 ETAT DU POINT 1
L'état du point 1 est donné figure ci-dessous. La pression est entrée, l'option "imposer la température de saturation" sélectionnée, avec un écart à la saturation égal à 5 K.
4.4.2 ETAT DU POINT 2s
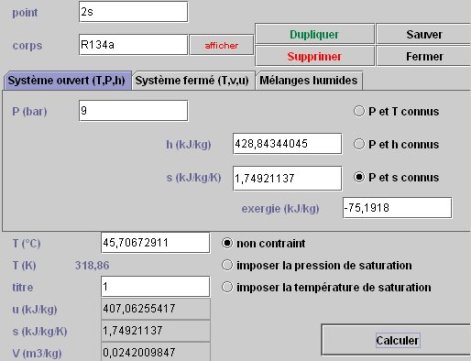
Pour connaître l'état du point 2s, le point doit être paramétré en mode de calcul « P et s connus », la nouvelle pression étant égale à 9 bars, et l'entropie étant celle du point 1. Le calcul conduit à la figure ci-dessous.
La valeur du travail de compression réel
 est, par définition du rendement isentropique
est, par définition du rendement isentropique
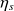 , égal à
, égal à
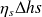 soit :
soit :
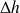 = 31,838/0,8 kJ/kg = 39,7975 kJ/kg
= 31,838/0,8 kJ/kg = 39,7975 kJ/kg
L'enthalpie du point 2 est donc égale à celle du point 1 plus
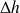 , soit 436,8025 kJ/kg.
, soit 436,8025 kJ/kg.
4.4.3 ETAT DU POINT 2
Pour connaître l'état du point 2, le point doit être paramétré en mode de calcul « P et h connus », la pression restant égale à 9 bars, et l'enthalpie valant 436,8025 kJ/kg. Le calcul conduit à la figure ci-dessous.
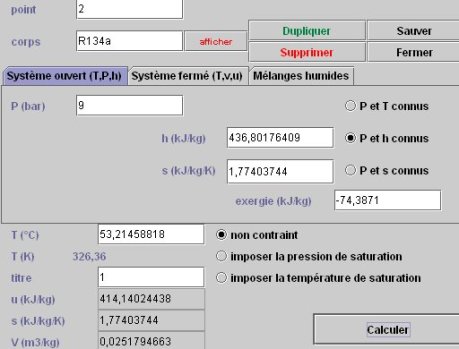
4.4.4 ETATS DES POINTS 3a ET 3b
Pour connaître l'état des points 3a et 3b, le paramétrage doit être "P et T connus", la pression restant égale à 9 bars, et la température de saturation étant imposée, x valant successivement 1 puis 0 avec un écart à la saturation de -5 K.
4.4.5 ETAT DU POINT 4
Pour connaître l'état du point 4, le paramétrage doit être « P et h connus », la nouvelle pression étant celle d'évaporation, égale à 2 bars, et l'enthalpie étant celle du point 3. Le calcul conduit à la figure ci-dessous. Le titre en sortie de turbine vaut 0,2716.
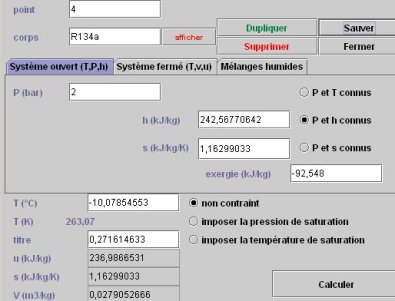
4.4.6 BILAN GLOBAL DU CYCLE
Les calculs précédents ont permis d'estimer la chaleur Q extraite à l'évaporateur (154,4 kJ/kg), et le travail de compression
 (39,8 kJ/kg).
(39,8 kJ/kg).
Le COefficient de Performance COP du cycle est égal au rapport de ces deux valeurs. Il vaut donc 154,4/39,8 = 3,89.
4.5 Modélisation directe dans Thermoptim
La modélisation directe du cycle dans Thermoptim est celle qui est présentée de manière détaillée dans le guide de prise en mains relatif au cycle de réfrigération et dans la séance Diapason S31 . Nous nous contenterons ici d'en rappeler les grandes lignes.
4.5.1 CREATION DU SCHEMA
Dans cette approche, l'élève commence par travailler avec l'éditeur de schémas, plaçant les différents composants sur la palette et saisissant pour chacun d'eux un tout petit nombre d'informations. Il aboutit ainsi à un schéma du type de celui présenté figure ci-dessous, qu'il transfère dans le simulateur : la seule différence avec le schéma-bloc est l'apparition des deux parties du condenseur, préalablement non distinguées.
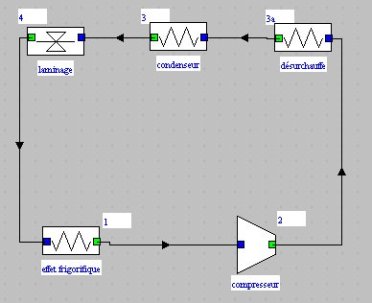
4.5.2 PARAMETRAGE DU CYCLE
Dans un second temps, l'élève paramètre sur le plan thermodynamique les points dont l'état est parfaitement connu (1, 3a, 3), et les transfos compression et laminage, ce qui permet de calculer les deux autres points.
4.5.3 COMPARAISON DES DEUX APPROCHES PEDAGOGIQUES
L'intérêt de la modélisation directe dans Thermoptim est qu'elle se fait dans un premier temps dans l'éditeur de schémas, l'architecture du cycle étant très proche de celle du schéma-bloc.
L'élève commence donc par réfléchir à la structure globale du cycle, sans avoir à se préoccuper de la manière dont les calculs sont effectués dans chaque composant. La modélisation est grandement facilitée, ce qui est un atout sur le plan psychologique, car l'élève est vraiment convaincu que le simulateur lui permet de "faire de la thermo sans peine". Il est donc encouragé à continuer, ses appréhensions initiales vis à vis de la discipline s'estompant.
Le risque est qu'il ait tendance à utiliser le logiciel de façon « presse-bouton », sans bien comprendre la méthodologie sous-jacente. Le parti pris pédagogique est donc assez différent de celui qui a été retenu dans les sections 2.3 et 2.4, où l'enseignant considère fondamental que l'élève ait pleinement conscience de l'enchaînement des calculs.
Dans tous les cas, les calculs sont effectués par un logiciel, ce qui correspond bien au même paradigme global, celui de la réduction des difficultés calculatoires, mais le degré d'implication de l'élève n'est pas le même. Les deux approches pédagogiques constituent donc des variantes entre lesquelles l'enseignant choisira, en fonction du contexte auquel il est confronté.
4.6 Représentation dans les diagrammes
Une fois les points du cycle déterminés, il est possible de le tracer dans les diagrammes usuels, notamment les diagrammes entropique, des frigoristes et de Mollier.
Dans ce qui précède, nous avions introduit les points 2s et 2, le premier étant un intermédiaire qui n'a pas besoin d'être représenté. Dans ce qui suit, pour simplifier les notations, nous n'afficherons que le point 2.
Si le cycle a été calculé en créant des points dans Thermoptim, comme expliqué dans les sections 4.3 ou 4.5, leur tracé dans les diagrammes peut être directement effectué en utilisant l'interface entre le simulateur et les diagrammes. S'il a été calculé avec le calculateur-inverseur, il faut commencer par créer les points dans le simulateur.
4.6.1 SAISIE DIRECTE DES POINTS DANS L'EDITEUR DE CYCLES
Il est possible d'enter directement les points dans l'éditeur de cycles du diagramme, en opérant de la manière suivante.
Une fois le diagramme des vapeurs du R134a ouvert, l'éditeur de cycles est accessible à partir du menu Cycle ou en tapant Ctrl C (figure ci-dessous).
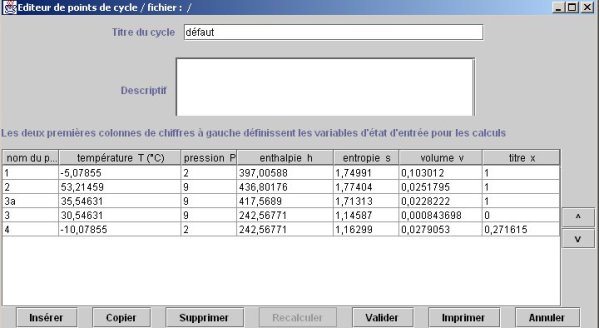
En utilisant le bouton Insérer, il est alors possible d'entrer les différents points un par un. La seule contrainte est que, le bouton de recalcul n'étant pas disponible dans la version Education Salle de cours de Thermoptim, il faut entrer à la main toutes les valeurs des variables (T, P, x, s et h) pour que le cycle soit correctement construit.
Notons qu'une fois ces points créés dans l'environnement des diagrammes, il est possible de les transférer dans le simulateur en utilisant l'interface qui les relie.
Dans l'écran de l'interface (figure ci-dessous), il faut commencer par mettre à jour la table des points, puis mettre à jour le simulateur à partir du diagramme.
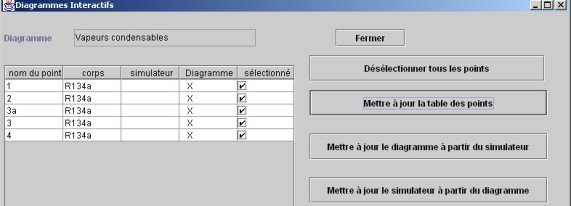
Les points sont alors créés dans le simulateur. Une fois ce transfert effectué, il est toutefois préférable de reprendre les paramétrages des points un par un, notamment pour imposer la température de saturation lorsque nécessaire.
4.6.2 TRACE DANS LE DIAGRAMME ENTROPIQUE
Sur le diagramme entropique (figure ci-dessous), pour augmenter la lisibilité, on n'a fait apparaître que les isobares (en bleu), et les isenthalpes (en rouge). Le point 1 légèrement surchauffé par rapport à la vapeur saturée est placé sur l'isobare 2 bars. La compression irréversible se traduit par une augmentation de l'entropie. Le refroidissement par l'air extérieur comporte trois étapes : une désurchauffe (2-3a) dans la zone vapeur, une condensation selon le segment de droite horizontal (3a-3b), et un léger sous-refroidissement (3b-3) presque confondu avec la courbe de saturation liquide.
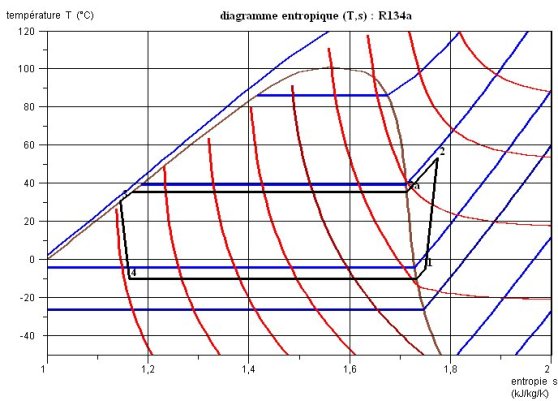
Le laminage isenthalpique (3-4) conduit à une une augmentation de l'entropie, le point 4 étant situé dans la zone d'équilibre liquide-vapeur (titre égal à 0,2716).
La forme de ce cycle s'écarte assez sensiblement de celle de celui de Carnot, compte tenu de l'allure des isobares. Il est possible de l'améliorer en procédant à des resurchauffes qui conduisent à une détente dite para-isotherme, et à des prélèvements qui permettent d'effectuer une régénération partielle. De telles variantes seront proposées aux élèves dans l'étape de consolidation de leurs connaissances (cf. troisième partie).
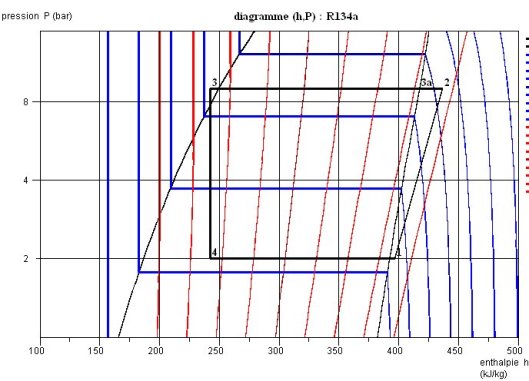
4.6.3 TRACE DANS LE DIAGRAMME DES FRIGORISTES
Sur le diagramme des frigoristes (h, log P) (figure ci-dessous), pour augmenter la lisibilité, on n'a fait apparaître que les isothermes (en bleu), et les isentropes (en rouge). La compression irréversible se traduit par une augmentation de l'entropie.
Si l'on néglige les pertes de charge dans le condenseur, l'ensemble du refroidissement correspond à l'horizontale (2-3), les trois parties représentant le désurchauffeur, la condensation proprement dite et le sous-refroidisseur apparaissant très distinctement.
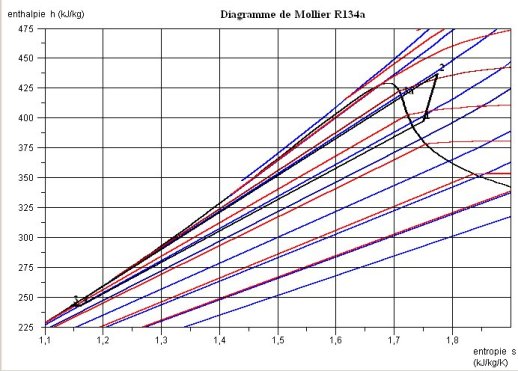
4.6.4 TRACE DANS LE DIAGRAMME DE MOLLIER
Sur le diagramme de Mollier (figure ci-dessous), pour augmenter la lisibilité, on n'a fait apparaître que les isobares (en bleu), et les isothermes (en rouge). Le point 1 légèrement surchauffé par rapport à la vapeur saturée est placé sur l'isobare 2 bars. La compression irréversible se traduit par une augmentation de l'entropie. Le refroidissement par l'air extérieur comporte trois étapes : une désurchauffe (2-3a) dans la zone vapeur, une condensation selon le segment de droite de pente T (3a-3b), et un léger sous-refroidissement (3b-3) presque confondu avec la courbe de saturation liquide.
4.7 Création dans Thermoptim des transfos à partir des points
Si le cycle a été modélisé sans utiliser l'éditeur de schémas de Thermoptim, (cf. sections 4.3 et 4.4), et que les points du cycle ont été créés ou transférés dans le simulateur afin de pouvoir les représenter dans les diagrammes, le projet se présente comme indiqué figure ci-dessous.
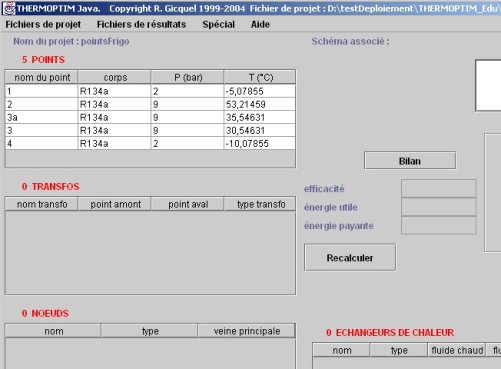
Pour finir de représenter le cycle dans Thermoptim, il faut maintenant relier ces points par des transfos, ce qui peut être fait très simplement à partir de l'éditeur de schémas. Il suffit pour cela de sélectionner dans la palette les différents composants, en entrant dans les champs définissant les ports d'entrée et de sortie leurs différents noms et leur corps (du R134a).
Les points étant tous connus, les transfos doivent être initialement paramétrées en conséquence. En particulier le compresseur doit recalculer la valeur du rendement, le point aval étant connu.
Une fois ces valeurs déterminées, le paramétrage peut être changé si l'on désire pouvoir simuler d'autres cas.
Le synoptique de l'installation se déduit des remarques précédentes (figure ci-dessous). Il correspond bien sûr au schéma de la figure de la section 4.5.1, auquel on a ajouté les sources de chaleur externes pour montrer que la machine interagit avec son environnement. On a aussi fait apparaître le cartouche avec le bilan du cycle, et on retrouve bien les valeurs qui avaient été déterminés par le calcul pas à pas.
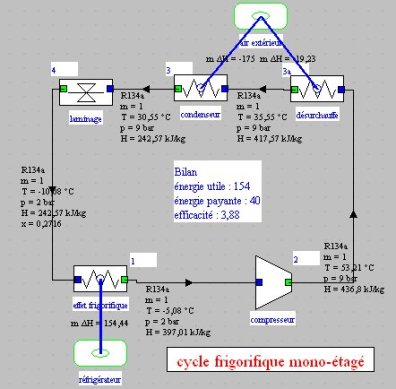
Ce cycle peut être directement obtenu en chargeant dans Thermoptim l'exemple intitulé « t1_6.2 cycle frigorifique simple » à partir du catalogue d'exemples.
4.8 Activités pédagogiques connexes avec les élèves
4.8.1 Diagrammes thermodynamiques
Des exemples d'activités concernant les diagrammes thermodynamiques sont donnés section 2.8.1. Nous vous suggérons de vous y reporter.
4.8.2 Cycle de machine frigorifique
Autour du cycle du réfrigérateur domestique, de nombreuses activités intéressant les élèves peuvent être proposées :
comparer qualitativement ce cycle par rapport au cycle de Carnot inverse, en identifiant les écarts qui existent entre eux ;
comparer la valeur du COP avec celle du cycle de Carnot inverse fonctionnant entre -5 °C (freezer) et 20 °C (air ambiant), pour se faire une idée de l'écart du cycle réel (3,88) par rapport au cycle idéal (11,7) ;
étudier l'évolution du COP et de la puissance frigorifique lorsque la température de l'air ambiant varie. Pour cela, il faut ajuster la pression de condensation pour que la température de condensation soit supérieure d'environ 15 °C à celle de l'air : environ 10,17 bars pour 25 °C, et 11,2 pour 30 °C. L'évolution du COP peut ainsi être tracée ;
étant donné que les points 3 et 4 ont la même enthalpie, plus le sous-refroidissement (3b-3) est important, plus l'effet frigorifique l'est, et ceci sans que le travail de compression soit modifié, comme le montre très bien le diagramme des frigoristes. On a donc intérêt à sous-refroidir autant que possible pour augmenter les performances du cycle. La limite est que la température du point 3 doit rester supérieure à celle de l'air extérieur, plus un certain écart, appelé pincement, nécessaire pour que la chaleur puisse être échangée ;
il est facile de fractionner la compression en deux phases, et de regarder quelle réduction du travail peut être obtenue par un refroidissement intermédiaire par échange avec l'air extérieur ;
le dimensionnement des sections de passage peut être déterminé en transformant le débit-masse en débit-volume à partir de la donnée du volume massique ;
il peut aussi être intéressant d'effectuer une comparaison de ce cycle avec celui utilisant le R12, fluide principalement utilisé auparavant dans les réfrigérateurs domestiques, mais banni depuis 1994 compte tenu de son important potentiel de destruction de la couche d'ozone. Cette comparaison montre que les niveaux de pression sont un peu modifiés, mais que le COP est sensiblement le même. Avec la version Education Salle de cours de Thermoptim, le changement de fluide se fait automatiquement à partir du Gestionnaire de corps (menu "Spécial"), tandis qu'avec la version de démonstration, il faut changer le nom du fluide dans l'éditeur de schémas puis mettre à jour le simulateur à partir de l'interface existante. On prendra garde à ce que les pressions doivent être modifiées pour que les températures de condensation et d'évaporation des deux cycles soient les mêmes.
4.9 Exploration de cycles existants
Dans ce qui précède, nous avons montré comment calculer pas à pas le cycle de la machine de réfrigération, puis comment le modéliser dans Thermoptim, en partant du principe que l'objectif pédagogique visé était d'apprendre aux élèves à acquérir ce savoir-faire tout en assimilant des connaissances déclaratives suffisantes pour comprendre les fondements de ces opérations.
Il existe cependant des contextes pédagogiques où cette manière de procéder ne peut pas être adoptée, essentiellement par manque de temps, et où cependant l'enseignant souhaite que ses élèves puissent utiliser Thermoptim et les diagrammes interactifs, sans construire par eux-mêmes les modèles.
C'est par exemple le cas dans certaines Classes Préparatoires aux Grandes Ecoles (CPGE) où le volume horaire est insuffisant pour opérer comme nous l'avons fait dans les sections précédentes. Pourtant, de nombreux enseignants considèrent pédagogiquement pertinent d'utiliser Thermoptim, car cela permet aux élèves de voir comment les équations qu'ils étudient peuvent être mises en application. Leur programme acquiert ainsi dans leur esprit davantage de sens : il correspond à un savoir qui peut être vraiment utilisé.
Dans de tels cas, une alternative pédagogique à celles que nous avons présentées jusqu'ici consiste à faire travailler les élèves sur des exemples déjà modélisés, en leur demandant de les explorer et de les comprendre. Ils peuvent aussi modifier les paramétrages et réaliser quelques études de sensibilité.
S'il souhaite faire étudier la machine de réfrigération de cette manière, l'enseignant sélectionne alors dans le catalogue d'exemples de Thermoptim l'exemple intitulé "t1_6.2 cycle frigorifique simple" à partir du catalogue d'exemples et demande à ses élèves de le charger.
Le projet étant chargé, il commence par passer en revue les différents composants, en fournissant à ses élèves des explications technologiques et thermodynamiques. Ensuite, il peut leur demander de procéder à des changements de paramétrage et d'en étudier l'impact sur les performances globales du cycle.
Même si elle peut paraître un peu limitée, cette approche pédagogique peut se révéler très féconde, les élèves s'impliquant souvent beaucoup plus lorsqu'ils ont un simulateur à leur disposition que devant une feuille de papier ou un tableau. Elle est en particulier souvent appropriée en formation professionnelle, les élèves étant généralement assez réticents devant les approches disciplinaires académiques. Ils préfèrent avoir l'outil logiciel entre leurs mains pour pouvoir l'explorer à leur guise et poser des questions aux enseignants qui les encadrent.
