Modèles de piles à combustible PEMFC
Remarque :
Une pile à combustible réalise une réaction électrochimique inverse de l'électrolyse : de l'hydrogène et de l'oxygène réagissent avec production d'électricité et d'eau et dégagement de chaleur, selon la réaction :
H2 + 1/2 O2 --> H2O
On voit ainsi que si le combustible utilisé est de l'hydrogène pur, la pile à combustible a pour seul sous-produit de l'eau : c'est un générateur particulièrement propre.
Le cœur de la pile est composé de deux électrodes, l'anode et la cathode, séparées par un électrolyte.
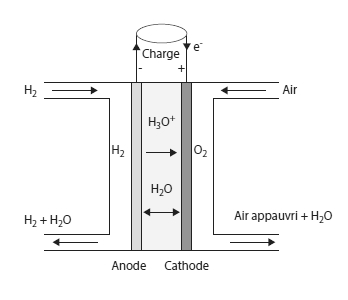
Dans certaines piles, comme les piles à oxydes solides (Solid Oxyde Fuel Cell ou SOFC en anglais), ce sont les ions oxydes O2- qui migrent de la cathode vers l'anode où l'eau est produite, et dans d'autres, comme les piles à membrane échangeuse de protons (Proton Exchange Membrane Fuel Cell ou PEMFC en anglais), ce sont des cations H3O+ (protons H+ hydratés) qui migrent de l'anode vers la cathode.
Dans une pile à membrane échangeuse de protons (PEMFC), ce sont les protons hydratés H3O+ qui migrent de l'anode vers la cathode, où l'eau est produite.
La faible tolérance au monoxyde de carbone d'une pile PEMFC impose que la concentration molaire de monoxyde de carbone CO du combustible soit inférieure à 10 ppm.
Modélisation d'une pile à combustible de type PEMFC
Pour modéliser une telle pile, plusieurs modèles de complexité croissante peuvent être réalisés, comme pour une pile SOFC. Les explications sont données données dans la page sur la pile SOFC et dans les séances Diapason S61 à S63.
Nous nous contenterons ici de détailler les trois étapes du reformage du méthane (séance S64) et les particularités de la pile PEMFC (séance S65):
vapocraquage catalytique : le vapocraquage catalytique est un procédé endothermique qui permet de transformer la molécule d'hydrocarbure en CO, CO2 et H2, en la faisant réagir avec de l'eau en quantité suffisante
réaction shift : la conversion du CO en CO2 se fait selon la réaction d'équilibre : CO + H2O <--> CO2 + H2 (modèle shiftCO aussi disponible séparément)
oxydation préférentielle : dans un réacteur PROX , une petite quantité d'oxygène est rajoutée au gaz de synthèse sortant du reformeur pour oxyder préférentiellement le CO en présence d'un catalyseur à base de platine
modèle de pile PEMFC : ce modèle utilise le reformat présenté ci-dessus


